
Frühe Daten von immatics lassen die Börse kalt
Die Tübinger Immatics N.V. stellte auf dem ESMO Immuno-Oncology Congress 2025 aktualisierte Daten aus der laufenden Phase Ia-Dosis-Eskalationsstudie zu ihrer PRAME-gerichteten Zelltherapie der zweiten Generation vor. Die überraschenden Ergebnisse haben kaum Auswirkungen auf den Aktienkurs. Möglicherweise liegt das an der Konkurrenz von zahlreichen Ansätzen gegen das PRAME-Zielmolekül (Preferentially Expressed Antigen in Melanoma), unter denen Immatics aber auch Immunocore (UK) schon in späteren klinischen Phasen unterwegs sind.
Auf dem ESMO Immuno-Oncology Congress 2025 stellte Immatics aktualisierte Daten aus der laufenden Phase Ia-Dosis-Eskalationsstudie zu seiner PRAME-gerichteten Zelltherapie der zweiten Generation (IMA203CD8) vor. Die Ergebnisse zeigen bei stark vorbehandelten Patienten mit PRAME-positiven soliden Tumoren ein handhabbares Sicherheitsprofil sowie erste Hinweise auf eine klinisch relevante, teils tiefe und anhaltende antitumorale Wirksamkeit.
IMA203CD8 ist eine weiterentwickelte TCR-T-Zelltherapie mit verbesserter Pharmakologie, die darauf abzielt, das therapeutische Potential der PRAME-Targetierung über das Melanom hinaus auf weitere schwer behandelbare solide Tumoren auszuweiten. Ein besonderer Fokus liegt dabei auf gynäkologischen Tumoren wie dem Ovarialkarzinom.
Studiendesign und Patientenkollektiv
In die laufende Phase Ia-Studie zur Dosis-Eskalation (NCT03686124) wurden bis zum Datenstichtag 27. Oktober 2025 insgesamt 78 stark vorbehandelte Patienten mit fortgeschrittenen oder metastasierten PRAME-positiven soliden Tumoren eingeschlossen. Die Patienten hatten zuvor im Median drei systemische Therapielinien erhalten und verfügten nur noch über begrenzte Behandlungsoptionen.
Über alle Dosisstufen hinweig zeigte IMA203CD8 ein insgesamt gut handhabbares Sicherheitsprofil. Auf Basis dieses Sicherheitsprofils wird die Dosis-Eskalation derzeit auf Dosisstufe 7 fortgeführt. Die Bestimmung der empfohlenen Phase II-Dosis (RP2D) ist für 2026 vorgesehen.
Antitumorale Aktivität und Dauerhaftigkeit des Ansprechens
Bereits bei vergleichsweise niedriger medianer Zellzahl zeigte eine einmalige Infusion von IMA203CD8 nach Unternehmensangaben eine „ermutigende antitumorale Aktivität“ über verschiedene PRAME-positive Tumorentitäten hinweg. Die objektive Ansprechrate lag bei 46%, die bestätigte objektive Ansprechrate bei 36%. Bei rund drei Viertel der behandelten Patienten wurde eine Tumorverkleinerung beobachtet, die Krankheitskontrollrate nach sechs Wochen betrug 84%.
Bemerkenswert ist die Tiefe und Dauer des beobachteten Ansprechens: Ein erheblicher Anteil der Responder zeigte eine Tumorreduktion von mindestens 50%, einzelne komplette Remissionen hielten über mehrere Jahre an. Die mediane Dauer des Ansprechens lag bei über 9 Monaten bei einer medianen Nachbeobachtungszeit von 14 Monaten.
Ein zentrales Ergebnis der vorgestellten Daten ist das dosisabhängige Wirksamkeitssignal beim Ovarialkarzinom. Bei Patientinnen, die höhere Dosisstufen erhielten, wurden bestätigte partielle Remissionen beobachtet, darunter auch eine anhaltende metabolische Komplettremission. Alle ansprechenden Patientinnen waren zuvor gegen platinbasierte Chemotherapien resistent. Die Verträglichkeit entsprach auch in dieser Subgruppe dem insgesamt beobachteten Sicherheitsprofil, und das Ansprechen trat ohne zusätzliche Gabe von niedrig dosiertem IL-2 nach der Zellinfusion auf.
Einordnung im PRAME-Portfolio von Immatics
Innerhalb der PRAME-Pipeline von Immatics baut IMA203CD8 auf den Erfahrungen mit anzu-cel, der Zelltherapie der ersten Generation auf, die im Melanom bereits hohe Ansprechraten in späteren Entwicklungsphasen gezeigt hatte. Sie befindet sich derzeit in der Phase III-Entwicklung und ist der Hoffnungsträger von immatics schlechthin. Mit seiner verbesserten Pharmakologie ist IMA203CD8 darauf ausgelegt, auch Tumoren mit heterogener PRAME-Expression und komplexerem Tumormikromilieu zu adressieren und damit das Einsatzgebiet zu verbreitern.
Das Tübinger Unternehmen verfolgt das Ziel, IMA203CD8 als tumoragnostische Therapieoption für fortgeschrittene PRAME-positive Tumoren zu positionieren, beginnend mit gynäkologischen Indikationen. Doch auch andere Unternehmen sind hier unterwegs, in Deutschland beispielsweise die Berliner T-Knife GmbH. Das deutsch-amerikanische Unternehmen plant, seine TCR-T Therapie der mittlerweile schon vierten Generation gegen PRAME, TK-6302, 2026 in die Klinik zu bringen. TK-6302 integriert Optimierungen für verbesserte T-Zell-Fitness, erhöhte Persistenz und einen skalierbareren Herstellungsprozess. Das Feld entwickelt sich zügig weiter. Designs der nächsten Generation der das Immunsystem stimulierenden Wirkstoffe und Zelltherapien sind auch andernorts in der Vorbereitung für klinische Studien oder bereits in der Klinik.
Vielleicht ist das ein Grund dafür, warum der Börsenkurs bei frühen Daten nicht sofort steil nach oben geht. Das Motto lautet wohl: abwarten, wer das Rennen wirklich macht.

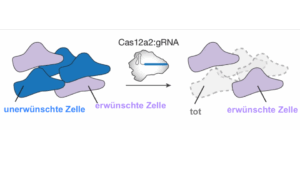 Scholz et al. https://www.nature.com/articles/s41586-026-10466-y/figures/4
Scholz et al. https://www.nature.com/articles/s41586-026-10466-y/figures/4 PathAI
PathAI Biontech SE
Biontech SE